Cơ chế phân tử điều chỉnh sự đông máu
Với việc áp dụng các kĩ thuật cắt lớp trong thao tác đơn phân tử, các nhà nghiên cứu thuộc đại học Harvard đã khám phá ra cơ chế phản ứng cơ bản của cơ thể trong việc điều chỉnh sự đông máu. Phát hiện này có thể dẫn tới mô hình dự đoán định lượng về cách cơ thể phản ứng với các vết thương, và là lời gợi ý cho phương pháp điều trị mới cho những rối loạn liên quan tới hiện tượng chảy máu.
Nhóm nghiên cứu do giáo sư Timothy A. Springer thuộc khoa Bệnh học trường Dược Harvard và bệnh viện Trẻ em Boston cùng Wesley P. Wong, Thanh Tra trưởng Viện Rowland tại Harvard mới đây đã công bố kết quả nghiên cứu về cơ chế phân tử của vòng phản hồi chịu trách nhiệm cho hiện tượng đông máu trên tờ Science số ra ngày 5 tháng 6 vừa qua.
“Cơ thể con người có một khả năng kì diệu để hàn gắn các vết bầm tím,” Wong giải thích. “Điểm chính của phản ứng này là khả năng làm ngừng hiện tượng chảy máu hay còn gọi là sự cầm máu. Tuy nhiên, cơ chế điều tiết cầm máu hiện vẫn là một hiện tượng cân bằng phức tạp.”
Đông máu quá nhiều có thể làm dư thừa các cục máu, rất có khả năng dẫn tới chứng nghẽn mạch gây tử vong. Ngược lại, nếu cơ thể đông máu quá ít, chúng ta có thể bị mất quá nhiều máu dẫn tới tử vong.
Để đạt được độ cân bằng hợp lý, cơ thể chủ yếu dựa vào một hệ thống phản ứng cơ học dựa trên các lực phân tử do hệ tuần hoàn tác động lên “cảm ứng lực” phân tử của vùng A2 trên protein đông máu mang tên von Willebrand factor (VWF).
Với việc điều khiển các phân tử đơn trên vùng A2 này, nhóm nghiên cứu đã phát hiện ra rằng vùng A2 hoạt động với vai trò như một bộ phận cảm ứng lực cực nhạy, phản ứng lại với những lực căng nhỏ nhất bằng cách mở ra và thu nhỏ cấu trúc ba chiều phức tạp của nó, cho phép enzyme ADAMTS13 thực hiện việc cắt nhỏ phân tử.
|
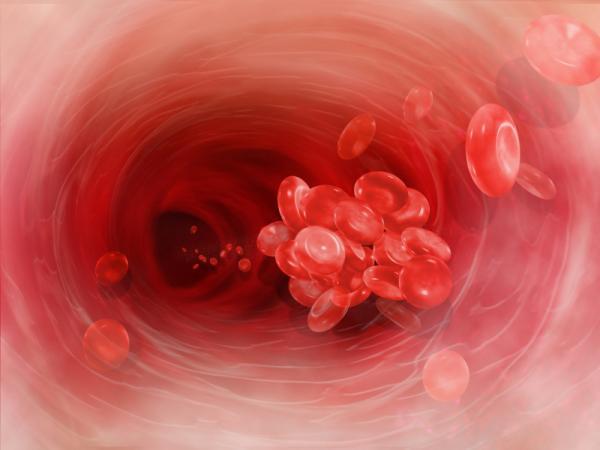
Các nhà nghiên cứu đã khám phá ra cơ chế phản ứng cơ bản mà cơ thể con người dùng để điều chỉnh quá trình đông máu. (Ảnh: iStockphoto/Rob Gentile) |
“Trong cơ thể, việc cắt nhỏ này làm giảm khả năng cầm máu và khiến các cục máu bị nhỏ lại về kích cỡ. Hệ thống này hoạt động hài hòa đến nỗi cảm ứng A2 có thể điều chỉnh kích thước của VWF trong dòng máu, duy trì kích thước tối ưu để phản ứng hợp lí trước các tổn thương của cơ thể,” Wong nói.
Công trình này đã góp phần mở rộng phạm vi hiểu biết của con người về cơ chế điều chỉnh sự hình thành các cục máu, cũng là một bước tiến mới dẫn tới mô hình dự đoán định lượng về phản ứng của cơ thể khi xuất hiện vết thương. Đồng thời, nghiên cứu này giúp hiểu rõ hơn về những rối loạn liên quan tới hiện tượng chảy máu, ví dụ như bệnh von Willebrand túyp 2A phá vỡ hệ thống điều chỉnh sự cầm máu, từ đó giúp tìm ra những cách điều trị và chẩn đoán mới.
Ngoài Wong và Springer, các tác giả của nghiên cứu bao gồm: Xiaohui Zhang, Kenneth Halvorsen, and Cheng-Zhong Zhang. Nhóm tác giả ghi nhận những đóng góp từ Viện Sức khỏe Quốc gia, Hiệp hội Tim Mạch Hoa Kỳ, và chương trình Đồng hành cùng Rowland.
Tham khảo:
Xiaohui Zhang, Kenneth Halvorsen, Cheng-Zhong Zhang, Wesley P. Wong, and Timothy A. Springer. Mechanoenzymatic Cleavage of the Ultralarge Vascular Protein von Willebrand Factor. Science, 2009; 324 (5932): 1330 DOI: 10.1126/science.1170905
Y học - Sức khỏe
-
Thí nghiệm khoa học cho thấy con người có thể không có ý thức tự chủ
-

Loài cây ra toàn trái độc nhưng thân lại là “mỏ vàng” trị giá bạc triệu, người Việt mua về để cầu tài lộc
-

Thành phố ngầm 10 triệu mét vuông lộ ra dưới lâu đài cổ nổi tiếng
-

Con người sẽ ra sao nếu một tiểu hành tinh có đường kính 1.000m và nặng 100.000 tấn va chạm vào Trái đất?
-

Loài cá 'bí ẩn': Có lúc còn 37 con, sống ở Hố Quỷ, chi phí bảo tồn lên tới hơn 90 tỷ đồng
-

Loại nước được ví như "viagra tự nhiên" giúp nam giới sung mãn bản lĩnh đàn ông
Đời sống
-

Giá dầu tăng, số người chết giảm
-

Kinh hoàng phát hiện ổ giòi trong lợi bé gái
-

Mắt - có thể mù lòa
-

Núi lửa Indonesia phun trào, hàng nghìn người sơ tán
-

Loại hoa được ví như "vương dược giải độc" và cách sử dụng đúng được lương y tiết lộ
-

WHO lo ngại tác dụng phụ từ vaccine H1N1 của Trung Quốc